Desde Washington (AFP)
Se retrasa aprobación de EEUU para vacunas de Moderna en adolescentes
La firma biotecnológica estadounidense Moderna informó el domingo que los funcionarios estadounidenses retrasaron la aprobación de su vacuna contra el covid-19 para adolescentes, con el fin de tener más tiempo para evaluar mejor el riesgo potencial de desarrollar miocarditis o inflamación cardíaca.
31 de octubre de 2021

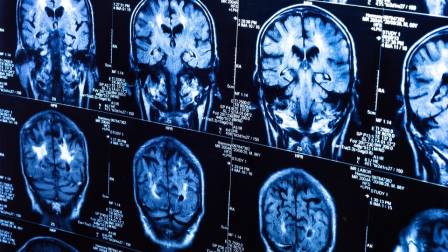
Esta foto de archivo tomada el 14 de octubre de 2021 muestra cajas que contienen dosis de la vacuna Moderna contra el covid-19, almacenadas en el Centro de Salud Comunitario Kedren en Los Ángeles, California. - AFP/AFP/Archivos
La firma biotecnológica estadounidense Moderna informó el domingo que los funcionarios estadounidenses retrasaron la aprobación de su vacuna contra el covid-19 para adolescentes, con el fin de tener más tiempo para evaluar mejor el riesgo potencial de desarrollar miocarditis o inflamación cardíaca.
La Administración de Drogas y Alimentos de Estados Unidos (FDA) "informó a Moderna que la agencia requiere tiempo adicional para evaluar los análisis internacionales recientes del riesgo de miocarditis después de la vacunación", explicó la compañía de biotecnología el domingo en un comunicado.
La evaluación para determinar si recomendar o no la vacuna de Moderna para jóvenes de 12 a 17 años podría durar hasta enero de 2022, anticipó la compañía.
La miocarditis y un riesgo asociado, pericarditis (inflamación alrededor del corazón), se han relacionado previamente con las vacunas contra el covid de Pfizer y Moderna, particularmente entre los adolescentes y los hombres jóvenes.
Sin embargo, el riesgo es mucho mayor después de la infección por covid-19, según un estudio publicado en agosto por los Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos.
El CDC encontró que "la miocarditis después de la vacunación con vacunas de ARNm ha sido inusual y generalmente leve", señaló Moderna.
Otra vacuna de ARNm contra el covid-19, de Pfizer-BioNTech, recibió el viernes la autorización de Estados Unidos para niños de cinco a 11 años, en dosis más pequeñas que para los adultos.
Moderna había dicho anteriormente que estaba esperando que la FDA decida si aprueba su vacuna para adolescentes menores de 18 años antes de buscar la aprobación del regulador para los grupos de edad más jóvenes.